在水晶學和礦物學中,晶體(Crystal)指的是一種固態物質,其內部原子、分子或離子以一種高度有序、三維重複的特定模式排列,形成一個規則的幾何結構。

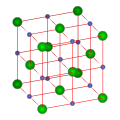
為了描述晶體的結構,我們把構成晶體的原子當成一個點,再用假想的線段將這些代表原子的各點連接起來,就繪成了像圖中所表示的格架式空間結構。這種用來描述原子在晶體中排列的幾何空間格架,稱為晶格。由於晶體中原子的排列是有規律的,可以從晶格中拿出一個完全能夠表達晶格結構的最小單元,這個最小單元就叫作晶胞。許多取向相同的晶胞組成晶粒,由取向不同的晶粒組成的物體,叫做多晶體,而單晶體內所有的晶胞取向完全一致,常見的單晶如單晶矽、單晶石英。大家最常見到的一般都是多晶體。
晶體的特性
晶體的分佈非常廣泛,自然界的固體物質中,絕大多數是晶體。氣體、液體和非晶物質在一定的適當條件下也可以轉變成晶體。晶體內部原子或分子排列的三維空間周期性結構,是晶體最基本的、最本質的特徵,並使晶體具有下面的通性:
- 長程有序 (Long-Range Order)
晶體內部的原子排列非常整齊,這種整齊的隊形會持續延伸到很遠的地方,至少在微米級別上保持不變。
- 均勻性(Homogeneity),即晶體內部各處宏觀性質相同;
核心概念是晶體內部各處的宏觀性質(例如密度、硬度、折射率等)都相同。因為晶體的原子排列是高度重複的,無論你從晶體的任何一點開始觀察,周圍的微觀環境都與其他點完全相同。這種微觀上的均勻性,使得整個晶體在宏觀上也表現出均勻的性質。
- 各向異性(Anisotropy),即晶體中不同的方向上性質不同;
核心概念是晶體中在不同方向上,其物理性質(例如光學性質、導熱性、硬度等)不同。這是晶體最迷人的特徵之一。因為晶體內部原子在不同方向上的排列間距和密度不同,所以當光、熱或力等作用於晶體時,其表現也會因方向而異。例如,某些晶體從不同方向看會呈現不同顏色(多色性),或者沿著某個方向更容易被劈開(解理)。
- 自限性 (Self-limitation)
- 在理想的生長環境中,晶體會自己長成一個帶有平整晶面的完整幾何體,不需要任何外力雕琢。
- 能自發形成多面體外形(Self-forming Geometric Shape);
核心概念是在理想的生長條件下,晶體會自發形成具有平整晶面、筆直稜角和尖銳頂點的幾何多面體。這種多面體外形是內部原子周期性排列在宏觀上的直接體現。晶面代表了原子排列最緊密、生長速度最慢的方向,使得晶體能夠沿著這些平面擴展,最終形成一個完美的幾何體。
- 有確定的、明顯的熔點(Fixed Melting Point);
核心概念是在給定的壓力下,晶體在一個固定的溫度下會從固態轉變為液態。由於晶體內部的原子排列高度有序,它們之間的鍵合能量是均一的。因此,當溫度達到一個特定值時,所有原子鍵會同時斷裂,導致晶體迅速融化。這與玻璃等非晶體不同,非晶體因為原子排列不規則,沒有固定的熔點,只會在一個溫度範圍內逐漸軟化。
晶體的對稱性不僅體現在外形上,更重要的是它反映了內部的原子排列。這就是為什麼晶體學家可以通過研究外部形狀,來推斷其內部結構。
- 有特定的對稱性;
晶體的外部形狀和內部原子排列都具有特定的對稱性,這種對稱可以被數學方式描述。核心概念是晶體具有反映、旋轉或反演等幾何操作的對稱性。解釋:晶體內部的原子排列是周期性的,這使得整個晶體具有可預測的對稱元素(如對稱面、對稱軸和對稱中心)。晶體學家正是利用這些對稱性來對晶體進行分類。
- 解理性 (Cleavage)
晶體能沿著某些特定的、平滑的晶面被劈開。這是因為在這些方向上,原子之間的連接力較弱。
- 最小內能 (Minimum Internal Energy)
在所有可能的排列方式中,晶體的原子排列是最穩定、能量最低的狀態。
原子就像一群小球,它們會自動找到最能穩定待在一起的排列方式。這種最穩定的排列,就是能量最低的狀態,也就是晶體的結構。這解釋了為什麼晶體比液體或氣體更穩定。
- 晶面角守恆 (Constancy of Interfacial Angles)
同種類的晶體,其對應的兩個晶面之間的夾角總是一個固定值,不會因為晶體的大小或形狀而改變。
- 能對X射線和電子束產生衍射效應等。
核心概念是當X射線或電子束穿過晶體時,會因其規則的原子排列而產生特定的衍射圖案。這是晶體學中最根本的應用之一。X射線或電子束的波長與晶體內部原子之間的間距相近,因此會與原子發生干涉,形成獨特的衍射圖案。通過分析這些圖案,科學家可以反向推導出晶體內部的精確原子排列結構。
為了更好地理解晶體,我們可以將它與非晶體(例如:玻璃、橡膠)做個比較。
|
特徵 |
晶體 (Crystal) |
非晶體 (Amorphous Solid) |
|
內部結構 |
高度有序的周期性排列 |
雜亂無序的隨機排列 |
|
熔點 |
固定、明確的熔點 |
沒有固定熔點,會在一定溫度範圍內軟化 |
|
外觀 |
在理想條件下,可形成規則的多面體 |
外觀不規則,沒有固定的幾何形狀 |
|
物理特性 |
具有各向異性 |
具有各向同性(各個方向性質都相同) |
晶體生長與缺陷
- 晶體缺陷
儘管晶體的原子排列很有規律,但現實中沒有完美的晶體。它們總會有一些小瑕疵(例如原子排列不對或缺了原子),這些瑕疵被稱為「晶體缺陷」。
多晶體
大部分工業用的金屬材料,並不是由一塊巨大的晶體構成,而是由很多很小的晶體(稱為晶粒)拼湊而成。這些晶粒之間的邊界就稱為「晶界」。
- 奈米晶體組裝
通常晶體是一個原子接一個原子慢慢長大的。但科學家發現,有些晶體(例如水鐵礦)是由很多微小的「奈米晶體」先長好,然後再像樂高積木一樣,自己拼湊成更大的晶體。這種特殊的生長方式,也會在晶體中留下獨特的缺陷。
晶體種類
晶體的結合力與特性
晶體的許多性質,都取決於將原子或分子黏合在一起的「結合力」。這些力量主要來自最外層電子(價電子)的相互作用。
結合力強:晶體會非常堅固,擁有較高的熔點。
結合力弱:晶體則會熔點較低,也比較容易變形或熔化。這類晶體通常只能在極低的溫度下形成。
四種主要的晶體類型
- 離子晶體:
結合方式:電子從一個原子轉移到另一個原子,形成帶正電和負電的離子,它們靠著異性相吸的電力(離子鍵)結合。
例子:食鹽(氯化鈉)。
- 共價晶體(原子晶體):
- 結合方式:原子之間共享價電子,形成極為強韌的共價鍵。
- 例子:鑽石、鍺和矽。這些電子能夠在原子間自由移動。
- 金屬晶體:
- 結合方式:金屬原子釋放出部分電子,形成帶正電的離子,並沉浸在由這些自由電子組成的「電子海洋」中。這些電子可以輕鬆從一個原子移動到另一個,形成電流。
- 例子:金屬。
- 分子晶體:
- 結合方式:分子之間不分享電子,而是靠著一種微弱的電力(范德華力或氫鍵)結合。由於這種力量很弱,這類晶體的熔點極低,硬度也極小。
- 例子:冰、固態氧。
人工晶體的生長方式
人工合成晶體是重要的工業技術。其中一種主要方法是「從熔液中生長」,常見於人造藍寶石、紅寶石和矽晶體的製造。
維爾納葉法(焰熔法):用來製造人造藍寶石和紅寶石。將氧化鋁粉末和少量上色用的粉末,在高溫火焰中熔化,然後滴到一顆「籽晶」上,讓它重新結晶,並承接籽晶的原子排列,形成一顆大的單晶體。
區域熔化法:用來純化半導體用的矽晶體。將一顆單晶體放在一根矽棒上方,在兩者接觸處加熱,使矽棒頂端熔化並在籽晶上重新結晶,然後將加熱區緩慢向下移動,從而得到高純度的單晶矽。
人造鑽石:由於鑽石形成條件嚴苛,需要超過 1600°C 和 60000 倍大氣壓的高溫高壓環境。目前生產的人造鑽石多為黑色細砂粒,主要用於工業用途。
晶體缺陷
什麼是晶體缺陷?
晶體缺陷指的是任何偏離晶體內部完美、週期性排列的因素。儘管名字叫「缺陷」,但它們並非總是壞事。事實上,它們對許多材料的性質有著決定性的影響。
重要:半導體的導電性、離子晶體的顏色、固體的強度等,都與晶體缺陷息息相關。根據缺陷的作用範圍,可以分為四類:
點缺陷:影響範圍很小,只在幾個原子位置上出現。
線缺陷:呈線狀,影響一整排原子。
面缺陷:呈面狀,影響一個較大的平面區域。
體缺陷:影響範圍大,像鑲嵌物、氣泡等。
缺陷的類型與成因
根據缺陷的形成原因,可以分為三大類:
- 熱缺陷(熱運動引起)
只要溫度高於絕對零度,晶體中的原子就會運動。當某些原子獲得足夠的能量,就會離開原本的位置,形成缺陷。
- 弗倫克爾缺陷(Frenkel Defect):原子離開原本位置,擠到晶格間隙中,形成一個空位和一個間隙原子。
肖特基缺陷(Schottky Defect):原子直接從晶體內部跑到表面,在原來位置留下空位。
- 組成缺陷(雜質引起)
當外來雜質原子進入晶體時,它們會破壞原有的週期性排列。
- 雜質原子可能取代原本的原子位置,也可能進入原子間的空隙。
- 例子:在矽(Si)中摻入磷(P)或硼(B),就是一種組成缺陷。這也是製造半導體的關鍵技術。
- 電荷缺陷(電子運動引起)
在非金屬晶體中,當電子獲得能量後,會從原本的位置(價帶)跳到新的位置(導帶),在原來的位置留下一個「電子電洞」。
- 影響:雖然原子排列沒有改變,但電子和電洞帶有正負電荷,會影響晶體的電場,從而產生缺陷。
- 半導體:這種缺陷是半導體導電的基礎。摻入磷(施主型雜質)會產生自由電子,形成 n型半導體;摻入硼(受主型雜質)會產生電子電洞,形成 p型半導體。
主要缺陷的詳細解釋
- 線缺陷(位錯)
這是一種非常重要的缺陷類型,被稱為位錯。它不是一條幾何線,而是原子排列發生滑動和變形的區域。位錯的存在對晶體的強度、生長和高溫下的特性有著巨大影響。
- 刃型位錯:想像晶體中多了一半層的原子,就像一把刀刃。其滑動方向與位錯線垂直。
- 螺旋型位錯:原子層沿著一個軸呈螺旋狀排列。其滑動方向與位錯線平行。
- 面缺陷
影響範圍是二維平面。常見的形式有:
- 晶界:在由許多小晶體組成的大塊材料中,不同小晶體(晶粒)之間的邊界就是晶界。晶界處的原子排列較為混亂,能量較高,是原子擴散的快速通道。
- 堆疊層錯:晶體層在堆疊時發生了錯誤的排列。
- 非化學計量化合物
這類化合物的原子數比例不符合簡單整數比。這也是一種由缺陷引起的現象。
- 原因:通常發生在能改變價態的元素(如鐵、鈦)氧化物中。當環境氣氛(例如還原或氧化)改變時,原子會離開或進入晶體,形成空位或間隙離子,從而改變整體的化學比例。
- 影響:這些缺陷會形成電子或電洞,使材料具有導電性,成為 n型或 p型半導體。
- 缺陷的符號與反應式
在學術研究中,科學家有一套專門的符號來描述這些缺陷,並用反應方程式來表達其形成過程。這些反應式必須遵循三個原則:
- 位置平衡
- 質量平衡
- 電價平衡
這套符號系統幫助科學家精確地描述晶體中複雜的缺陷現象。
晶體軸的定義與作用
- 人工座標軸:ABC軸是為了方便描述晶體結構而設立的假想直線。
- 對應晶胞參數:這三個軸的方向與晶胞的邊長(a、b、c)方向平行。
- 右手座標系:它們組合成一個右手座標系,方便描述晶體中的位置和方向。
- 定義晶面和晶向:晶體軸系統用於定義晶面(晶體表面的法線方向)和晶向(晶體內部原子排列的方向)。
為什麼晶體會有不同的特性?常見晶體是怎麼被黏在一起的?
第一點:晶體特性的「黏著力」
想像一下,每個原子或分子都是一顆積木,而將它們黏在一起的,就是「結合力」。如果這個「黏著力」非常強,積木牆就特別堅固,很難拆開。這類晶體通常熔點高,也不容易彎曲變形。
如果「黏著力」很弱,積木牆就很脆弱。這類晶體熔點低,很容易就融化了,甚至只有在非常冷的環境下才能形成。
第二點:晶體的主要「黏著劑」
將積木黏在一起的方式有很多種,但這些方式並不會決定積木一定會排列整齊。不過,我們可以歸納出一些常見的趨勢:
- 金屬鍵(金屬晶體): 金屬原子就像一群人,他們把自己的東西(電子)都拿出來,在一個公共空間裡自由共享。這些電子在原子周圍自由移動,形成一股「電子海」,把帶正電的原子牢牢黏在一起。
- 離子鍵(離子晶體): 離子化合物的原子就像是異性相吸的男女。一個原子把電子完全給了另一個原子,自己變成帶正電的「陽離子」,對方則變成帶負電的「陰離子」。兩種不同電性的粒子就靠著這個強大的電力,緊緊地結合在一起。食鹽(氯化鈉)就是最典型的例子。
- 共價鍵(共價晶體): 這是一種最穩定的「黏著」方式。原子之間不會轉移電子,而是彼此共享電子,形成一個極為強韌的共用連接。鑽石就是用這種方式,每個碳原子都和周圍的四個碳原子緊密相連,這使得它成為地球上最硬的物質之一。
- 范德華力(分子晶體): 這是一種最微弱的「黏著」方式。分子本身不共享電子,但因為分子內電荷分佈不均,會在一端形成微弱的負電,另一端形成微弱的正電。這就像兩塊小磁鐵,微弱的電力會讓它們互相吸引,但這股力量非常小。這就是為什麼固態氧和冰的熔點都非常低的原因。
晶系與ABC軸的關係
ABC軸的長度、相互夾角和垂直性決定了晶體的「晶系」。 這六種基本晶系(三斜、單斜、正交、四方、六方和立方)反映了晶體在空間中的對稱性。- 立方晶系(等軸晶系):a=b=c,軸間角均為90°。
- 四方晶系(正方晶系):a=b≠c,軸間角均為90°。
- 正交晶系(斜方晶系):a≠b≠c,軸間角均為90°。
- 單斜晶系:軸角α=γ=90°,β>90°。
- 三斜晶系:所有軸角均非90°。
- 六方和三方晶系:: 在某些定義中會使用X、Y、U、Z四個座標軸來描述,其中水平軸間夾角為120°,Z軸直立。
晶系的特徵與細分關係如下表:
| 晶族 | 晶系 | 點群的對稱性 | 點群 | 空間群 | 布拉菲晶格 | 特徵 | 晶格系統 |
|---|---|---|---|---|---|---|---|
| 三斜 | 無 | 2 | 2 | 1 | α≠β≠γ≠90°,a≠b≠c | 三斜 | |
| 單斜 | 1個兩次對稱軸 或 1個對稱面 | 3 | 13 | 2 | α=γ=90°,β≠90°,a≠b≠c | 單斜 | |
| 正交/斜方 | 3個兩次對稱軸 或 1個兩次對稱軸+2個對稱面 | 3 | 59 | 4 | α=β=γ=90°,a≠b≠c | 正交/斜方 | |
| 四方/正方 | 1個四次對稱軸 | 7 | 68 | 2 | α=β=γ=90°,a=b≠c | 四方/正方 | |
| 六方 | 三方 | 1個三次對稱軸 | 5 | 7 | 1 | α=β=γ≠90°,a=b=c | 三方 |
| 18 | 1 | α=β=90°,γ=120°,a=b≠c | 六方 | ||||
| 六方 | 1個六次對稱軸 | 7 | 27 | ||||
| 立方/等軸 | 4個三次對稱軸 | 5 | 36 | 3 | α=β=γ=90°,a=b=c | 立方/等軸 | |
| 6 | 7 | 共計 | 32 | 230 | 14 | 7 | |








沒有留言:
張貼留言